
Autor: Joe Hylton, MA, BSRT, RRT-ACCS/NPS, NRP, FAARC, FCCM, especialista en aplicaciones clínicas, Hamilton Medical Inc.
Fecha: 15.07.2021
La capnografía de forma de onda es un procedimiento habitual en la medicina de cuidados intensivos. Se trata de una herramienta de validación del control de la vía aérea ampliamente utilizada y con mucho predicamento en los entornos de sedación consciente, así como durante los traslados entre instalaciones de pacientes intubados que requieren ventilación mecánica. La capnografía de forma de onda puede proporcionar información oportuna y muy valiosa a un profesional sanitario con la debida formación.

Hay infinidad de factores que pueden afectar a la cantidad de dióxido de carbono en el gas al final del volumen tidal (PetCO2). Respecto a la eliminación de CO2, existe un estrecho equilibrio continuado entre la producción de CO2 en los tejidos, su transporte por la sangre, la difusión hacia los alveolos y la eliminación por ventilación (
Un aumento o disminución de la tasa metabólica del paciente conllevaría un cambio en la producción de CO2 y, por tanto, también en la eliminación de CO2. Si tanto la circulación como la ventilación son estables —estado que solo pueden alcanzar los pacientes con ventilación mecánica pasivos—, la monitorización del CO2 se puede usar como indicador de la producción de CO2. La fiebre, la septicemia, el dolor o las convulsiones son todos cuadros que pueden aumentar la actividad metabólica, lo que conlleva el correspondiente aumento de la producción de CO2 y, por tanto, un valor de PetCO2 mayor. Por el contrario, la actividad metabólica disminuye en pacientes con hipotermia, sedados o paralizados. Esto reduce la producción de CO2 y puede desembocar en una disminución del valor de PetCO2 si la ventilación minuto no aumenta al mismo tiempo (
El transporte de CO2 a los pulmones depende de una correcta función cardiovascular. En consecuencia, cualquier factor que altere la función cardiovascular puede influir también en el transporte de CO2 a los pulmones (
La expulsión del CO2 de los pulmones al entorno exterior se ve afectada por los cambios en la función respiratoria. Las enfermedades pulmonares obstructivas, la neumonía, los trastornos neuromusculares y los trastornos del sistema nervioso central que alteran la función respiratoria tendrán pues el correspondiente efecto modificador del valor de PetCO2 (
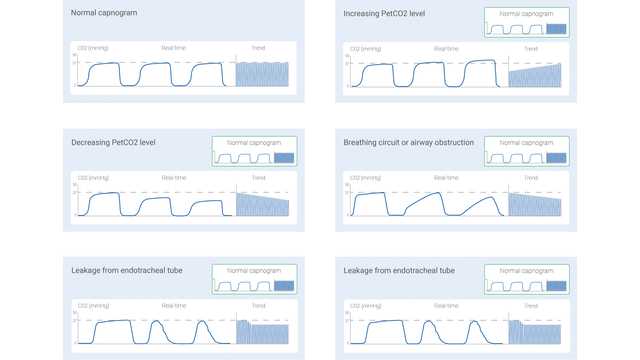
La señal de CO2 medida se puede registrar como una función de tiempo (capnografía temporal) o como volumen espirado (capnografía volumétrica). La cantidad de información que estos dos tipos de capnografía pueden proporcionar varía notablemente. En algunos estudios se han descrito algunas formas de los capnogramas temporales consideradas como típicas de situaciones clínicas específicas. En la figura 1 de abajo se muestran algunas de las más habituales.
Con todo, la capnografía temporal también tiene sus limitaciones: no puede dar una estimación precisa del estado de ventilación-perfusión de los pulmones, y tampoco se puede usar para calcular el componente de espacio muerto fisiológico. La capnografía volumétrica, pese a no ser tan sencilla y cómoda como la capnografía temporal, tiene la ventaja de que ofrece una cantidad de información considerablemente mayor.
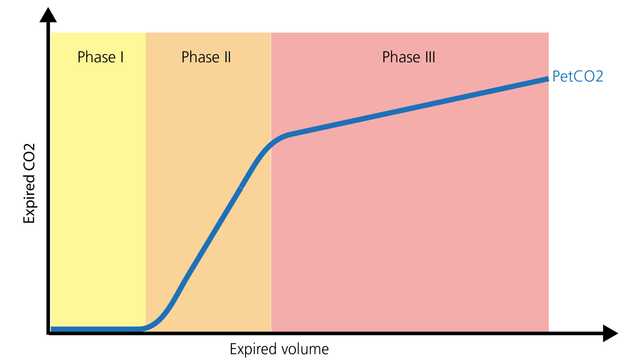
La forma normal de un capnograma volumétrico consta de tres fases. Es importante recordar que el capnograma representa una espiración.
La capnografía, tanto si es temporal como volumétrica, puede arrojar información muy valiosa para optimizar la monitorización y guiar los cuidados de pacientes que deben trasladarse a otra zona del hospital o a otro hospital. Se puede utilizar de forma segura con tubos endotraqueales, tubos de traqueotomía y numerosas vías aéreas supraglóticas, siempre y cuando haya un sellado eficaz. La colocación y permeabilidad de la vía aérea, la monitorización de la ventilación y el estado de la perfusión son todos ámbitos en los que el valor de PetCO2 proporciona información significativa. Otro parámetro muy útil es el volumen de dióxido de carbono eliminado por minuto (V'CO2), que permite a los profesionales sanitarios valorar los esfuerzos efectivos de reanimación de volumen y perfusión (
En las unidades de cuidados intensivos, la capnografía de forma de onda permite seguir monitorizando la colocación y permeabilidad de la vía aérea, con los correspondientes dispositivos complementarios de vía aérea. La relación existente entre el espacio muerto anatómico y el volumen tidal (VD/Vt) es una medición de capnografía importante. Una relación VD/Vt en aumento puede representar un posible incremento de la mortalidad dependiendo del nivel de aumento (
Todos los respiradores de Hamilton Medical incorporan capnografía volumétrica (
Aprenda a interpretar capnogramas volumétricos y obtenga una visión general de las ventajas y las aplicaciones clínicas de la capnografía volumétrica. Incluye una prueba de autoevaluación.